La cohésion d'un solide ionique est assurée par :
des liaisons hydrogène.
des interactions électrostatiques.
des liaisons covalentes.
Pour réviser cette notion, voir le cours 1 : Cohésion dans un solide.
Les liaisons de Van der Waals et les liaisons hydrogène s'exercent :
entre les ions d'un solide ionique.
entre les molécules d'un solide moléculaire.
entre deux atomes d'hydrogène.
Pour réviser cette notion, voir le cours 1 : Cohésion dans un solide.
Dans un cristal ionique :
il y a toujours autant de cations que d'anions.
il y a toujours autant de protons que d'électrons.
la cohésion est assurée par des liaisons hydrogène.
Pour réviser cette notion, voir le cours 1 : Cohésion dans un solide.
La liaison hydrogène s'établit :
entre un cation et un anion.
entre des atomes de charges partielles opposées.
entre des molécules apolaires.
Pour réviser cette notion, voir le cours 1 : Cohésion dans un solide.
Parmi ces étapes, laquelle ou lesquelles sont des étapes de la dissolution d'un cristal ionique ?
La dilution.
La dispersion.
La solvatation.
Pour réviser cette notion, voir le cours 2 : Dissolution d'un solide ionique.
Les étapes de dissolution d'un solide ionique sont, dans l'ordre :
hydratation, dispersion, solvatation.
dissociation, solvatation, dispersion.
solvatation, hydratation, dispersion.
Pour réviser cette notion, voir le cours 2 : Dissolution d'un solide ionique.
Les indices respectifs pour le soluté et les ions en solution sont :
(aq) et (s).
(s) et (aq).
(s) et (𝓵).
Pour réviser cette notion, voir le cours 2 : Dissolution d'un solide ionique.
L'équation de dissolution de Fe2(SO4)3(s) est :

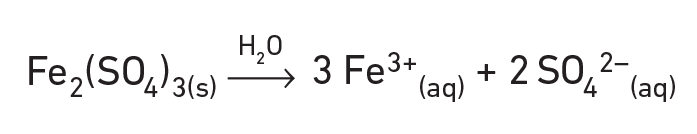

Pour réviser cette notion, voir le cours 2 : Dissolution d'un solide ionique.
Dans le solvant extracteur, le soluté doit être :
soluble.
miscible.
insoluble.
Pour réviser cette notion, voir le cours 3 : Solubilité d'une espèce dans un solvant.
Lors d'une extraction liquide-liquide, les deux solvants doivent être :
solubles.
non miscibles.
insolubles.
Pour réviser cette notion, voir le cours 3 : Solubilité d'une espèce dans un solvant.
Un soluté polaire est soluble dans :
un solvant polaire.
un solvant apolaire.
un solvant où s'établissent des liaisons hydrogène.
Pour réviser cette notion, voir le cours 3 : Solubilité d'une espèce dans un solvant.
L'espèce active d'un savon contient des ions qui sont :
des cations.
amphiphiles.
hydrophiles.
Pour réviser cette notion, voir le cours 3 : Solubilité d'une espèce dans un solvant.
L'ion carboxylate RCOO– est :
soluble dans l'eau.
insoluble.
soluble dans l'huile.
Pour réviser cette notion, voir le cours 3 : Solubilité d'une espèce dans un solvant.
 QCM
QCM